Classificazione
Odefseyè un farmaco monouso a dose fissa combinato utilizzato nel trattamento dell’HIV, che comprende tre diversi agenti antiretrovirali:
- rilpivirina, un non- inibitore nucleosidico della trascrittasi inversa (NNRTI)
- emtricitabina, un inibitore nucleotidico della trascrittasi inversa (NtRTI)
- tenofovir alafenamide (TAF), un altro NtRTI
Odefsey è la seconda combinazione di farmaci ad usare TAF, una versione "migliorata" di tenofovir disoproxil fumarato (TDF) trovato nelle droghe Truvada e Atripla.
Come tale, può essere considerato un miglioramento di Complera, la formulazione a compressa singola composta da rilpivirina + emtricitabina + TDF.
TAF è considerato superiore al TDF in quanto è in grado di erogare il farmaco attivo più efficacemente alle cellule e a dosi molto più ridotte, il che significa che c’è meno accumulo del farmaco nel sangue e molto meno possibilità di sviluppare tossicità renale correlate al farmaco . While (Mentre il rischio di tossicità renale associata a TDF è considerato basso nei paesi sviluppati, tale rischio è visto aumentare considerevolmente nei paesi in via di sviluppo dove vi è una maggiore incidenza di disfunzione renale preesistente.)
Indicazione del trattamento
Odefsey è stato approvato da la Food and Drug Administration degli Stati Uniti il 1 ° marzo 2016 per l’uso sia negli adulti che nei bambini di età superiore ai 12 anni che non hanno mai partecipato alla terapia dell’HIV, che hanno una carica virale di 100.000 cellule / me inferiore e pesano 77 libbre (35 kg ) o più.
Odefsey può anche essere usato per sostituire una terapia corrente (come quelli su Complera) se il paziente ha avuto una carica virale non rilevabile (<50 cellule / ml) per almeno sei mesi, non ha storia di fallimento del trattamento e non ha resistenza nota a qualsiasi farmaco componente in Odefsey.
Formulazione
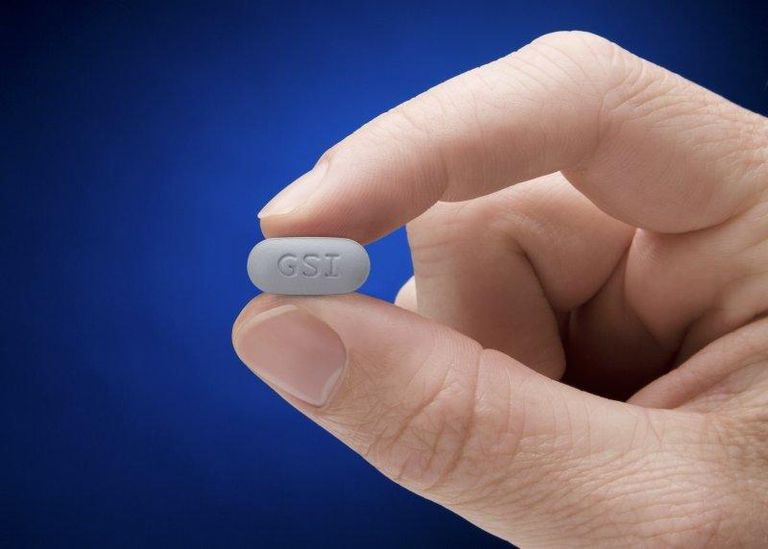
Odefsey è una compressa grigia, oblunga, rivestita con film, composta da 25 mg di rilpivirina, 200 mg di emtricitabina e 25 mg di TAF.
È impresso con "GSI" su un lato e con un "255" sull’altro.
Dosaggio
Una compressa al giorno presa con il cibo. Odefsey non deve essere assunto con altri farmaci antiretrovirali usati per il trattamento dell’HIV.
Effetti collaterali
Un certo numero di effetti collaterali sono stati osservati in pazienti in trattamento con rilpivirina e / o emtricitabina + TAF, i più comuni dei quali:
Nausea
- Mal di testa
- Insonnia
- Depressione
- Gli effetti collaterali erano generalmente transitori, con pochi pazienti che hanno interrotto l’intolleranza al trattamento.
Controindicazioni
Odefsey dovrebbe
non essere presa con i seguenti farmaci o integratori: Farmaci anticonvulsivi: Tegretol, Trilepta, fenobarbital, fenitoina
- Farmaci anti-tubercolosi: Mycobutin, Rifater, Rifamate, Rimactane, Rifadin, Priftin
- Inibitori della pompa protonica (PPI): Nexium, Kapidex, Dexilant, Prevacid, Losec, Prilosec, Protonix, Aciphex o qualsiasi altro PPI
- Farmaci steroidei: desametasone (anche se può essere somministrato in una singola dose, se clinicamente indicato)
- St Erba di San Giovanni
Informare sempre il medico di qualsiasi farmaco o integratore, prescritto o non prescritto, che potrebbe essere assunto prima di iniziare qualsiasi terapia antiretrovirale. - Altre considerazioni
Odefsey non è raccomandato per i pazienti con compromissione renale (definita come una clearance stimata della creatinina inferiore a 30 ml al minuto).
Informi il medico se è stato o è in trattamento per un disturbo renale da un altro medico.
Odefsey non è raccomandato per pazienti con insufficienza epatica o per pazienti con infezione da epatite B (HBV) cronica poiché può esacerbare gravemente problemi al fegato. È consigliabile che le persone con HIV siano sottoposte a screening per HBV prima di prescrivere Odefsey. Si prega di avvisare il medico se si hanno problemi al fegato e / o anamnesi positiva per epatite.
La componente rilpivirina di Odefsy può causare una reazione di ipersensibilità in un piccolo numero di pazienti, spesso sotto forma di eruzioni cutanee, infiammazione degli occhi ("occhi rosa"), gonfiore facciale, febbre o altre reazioni allergiche.
Tipicamente, le reazioni di ipersensibilità si presentano 1-6 settimane dopo l’inizio della terapia. Informare immediatamente il medico di tali sintomi. Nei casi più gravi, è probabile che la terapia debba essere interrotta.